|
牛肺疫 (contagious bovine pleuropneumonia: CBPP)
|
|||||||||
|
FAO Animal Health Manual No. 14「牛肺疫 (CBPP) 緊急対応準備計画策定の手引書」から
"第 2 章 牛肺疫 (CBPP) の特徴" を抜粋して掲載 阿部 香里 訳 |
|||||||||
牛肺疫とは、牛の急性、亜急性、もしくは慢性のマイコプラズマ感染症で、著しい生産性低下と死亡率の上昇を引き起こす。繊維素性肺炎、繊維素性胸膜炎、小葉間間質の浮腫が特徴である。 |
|||||||||
世界分布 牛肺疫は、現在、主にアフリカの疾病であり、アフリカでは最も深刻な越境性動物疾病と考えられている。本病はサハラ以南アフリカのほとんどの国に常在しており、そのうち少なくとも 27 ヵ国は牛肺疫の存在を報告している。例外は南部アフリカの数ヵ国?ボツワナ、マラウイ、モザンビーク、南アフリカとジンバブエ、そして北部の国境付近以外のナミビア全土である。1990 年代は特にアフリカにおいて牛肺疫の感染が増加し、それまではかなり長期的にわたって本病の発生が認められなかった東部アフリカと南部アフリカの一部において再び深刻な牛肺疫の感染が広まった。これは 1995 年のボツワナ北部の感染でピークに達した。ボツワナは摘発淘汰によって疾病を撲滅し、1997 年 1 月には暫定的に撲滅されたと宣言した。 牛肺疫は地中海沿岸のいくつかの国でも 1990 年代には存在していた (イタリア 1993年、スペイン 1994 年、ポルトガル 1999年)。 この疾病はアジアの一部にもまだ存在するかもしれないが、未確認である。バングラデシュは公式に牛肺疫の存在を確認している唯一の国である。その他の大陸には存在しない。 |
|||||||||
病原体 牛肺疫 (CBPP) の病原体は小コロニー株 (牛型) (MmmSCと略す ) の Mycoplasma mycoides subsp. mycoides である。これは反芻動物に対して大なり小なり病原性のある6種の近縁なマイコプラズマを含む「mycoides グループ」に属する。このグループの血清学的及び遺伝子的関連度は高い。MmmSC の血清型は1つだけである。 MmmSC は他のマイコプラズマ同様、細胞壁を欠き、多形性である。新しい培養においては枝上構造をとることが多いが時間が経った培養では小球菌状である。発育にはコレステロールを多量に含む特殊な (血清添加) 培養基を必要とする。本病原体は弱く、宿主の体外ではほとんど生存できない。乾燥及び消毒に対し感受性である。 |
|||||||||
感受性家畜 (Susceptible species) 牛肺疫は主に牛の疾病である。Bos taurus とBos indicus の両種は完全に感受性である。水牛は感受性がやや低い。牛肺疫はヤクとバイソンにも感染することが報告されている。ラクダ、野生のウシ科動物及びその他の反芻動物は抵抗性がある。本病の病原体は羊と山羊からも分離されているが、これらの動物が牛肺疫の伝播に何らかの役割を果たしているという証拠はない。 |
|||||||||
疾病感染 この疾病は感染家畜と感受性家畜との直接の接触によってのみ、感染した煙霧質により空気感染する。約 200 m 範囲内の空気感染が可能と考えられている。放牧密度の高い牛群ほど急速に感染が広まる可能性が高い。微徴候で慢性的に感染している動物は新しい地域に疾病を広める重要な役を担う。 慢性牛肺疫保持家畜は一見健康であり、肺の中の繊維状莢膜にシーケストラム (複数形=シーケストラ) を形成する肺病変を持っている。そのような家畜はよく「肺保菌牛 (lungers)」と呼ばれている。病原体はそのような状態で何ヵ月も潜伏し、繊維状莢膜が壊れた時に病原体は気管支を通り肺から飛び出し感受性の家畜を感染発病させる。これは特に慢性的な牛肺疫キャリアーの動物が長距離の徒歩による移動や輸送等のストレスにさらされる際にしばしば起こる。マイコプラズマは宿主の体外で生存する能力は弱いので、(嘔吐物などによる) 間接感染はここでは重要ではない。 |
|||||||||
疾病パターン 流行性牛肺疫はこの疾病がこれまでは無感染であった地域や国、もしくは群に感染した時におこる。このタイプの特徴は群の中での高い感染率、それも急性型感染家畜が多く、致死率も高い。群中、もしくは群間の感染率は、特に家畜が多く集まる水のみ場や家畜市などの機会、そして家畜群を市場へ連れていく途中や囲い込んだりする際に特に高い。 突発発生の初期段階においては、感染密度は低く、感染の広がり方は遅いかもしれない。そのような状況の場合、感染がピークを迎えるまで数ヵ月かかることもありうる。この初期の段階は、早期認知と疾病検疫の面で特に危険な段階である。感染潜伏期間がまちまちで、しばしば潜伏期間が長いことや、疾病は一見健康そうに見える動物から感染が広まることから、疾病がいつどの時点で突発したのか感染経路を突き止めることは難しいことが多い。 この状態で疾病が効果的に抑制されないかぎり、ゆくゆくは牛肺疫が蔓延化し、これが多くのアフリカ諸国の現状である。蔓延化した牛肺疫の感染は偶発的であり、多くの場合は軽症で慢性的な状況で致死率も低い。時々感染が大流行する場合もあるし、全体的にみれば、このような慢性化状態でもかなりの家畜生産の損失を招く。 |
|||||||||
|
|||||||||
臨床症状 潜伏期間は一般的に 3 から 6 週間であるが、最長 6 ヵ月ほど長期にわたることもある。急性型の場合は 3 日から 10 日の発熱、食欲不振, 乳牛の場合は牛乳生産の低下、著しい沈うつ症状そして通常は腹部の呼吸の乱れなどがみられる。これらはすぐに乾いた咳に変わり、それが段々と激しくなり、典型的には風に向かって背中を丸め、ひじを突き出し、頭を伸ばしている姿から胸部の痛みを感じているのが分かる。時には血液まじりの鼻汁や口の周りに泡状の涎がたまることもある。重症の場合の致死率は 75 %にも昇り、疾病の兆候が現れてから 3 月以内に致死に至る。回復した動物でも非常に弱く削痩した状態であり、慢性的キャリアーとなるものが多い。発生の初期段階では極度の急性パターンも発生することがあり、その際はいくつかの微かな兆候で突然死亡に至ることもある。 一般的なものは亜急性もしくは慢性的なケースである。その際の兆候は穏やかで、兆候が確認されない場合もある。微熱、体重減少、呼吸器症状は、その対象動物が激しい運動をして初めて兆候が分かる。不顕性なケースもありうる。 6 ヵ月未満の子牛の場合、牛肺疫は関節炎としてしか現れない。その際は跛行と関節の柔らかい腫れが見られる。 |
|||||||||
|
|||||||||
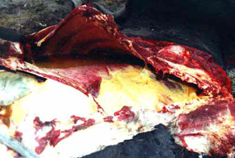
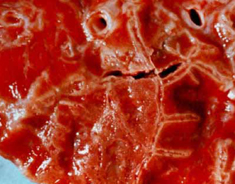
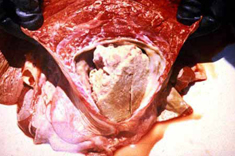
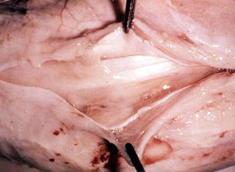
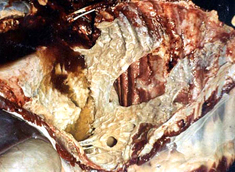
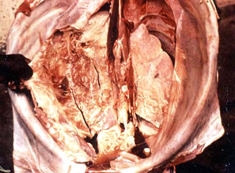
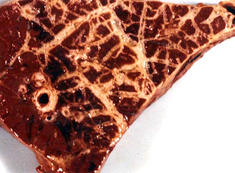
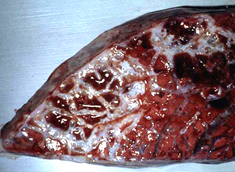
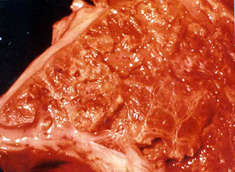
病理解剖所見 牛肺疫の急性型では繊維素性肺炎と夥しい量の胸水が認められる。特に後者は驚くほどの量の、30 リットルにも及ぶ黄色い滲出液で凝塊を含み胸郭内に貯留する。肺は片側性または両側性、部分的または全体的に硬化し特徴的な大理石紋様が認められる。病変部は腫脹し、桃色から暗赤色の様々な色調を呈し、やや硬い質感となり、透明な液体が滴る。時に切断面から出た血が混じることがある。小葉間中隔は著しく肥厚する。感染部位を覆う胸膜表面は肥厚し、灰色から赤色を呈し、しばしば、黄色くもろい繊維素に覆われる。局所のリンパ節は腫脹し、浮腫状を呈し、壊死が認められることがある。 慢性型では、壊死した肺組織が包囲されて直径 1-20 cm のシーケストラムを形成する。シーケストラム内の組織は、元の急性型の肺病変の構造を保つ傾向があるが、時間が経つにつれて石灰化や液状化することもある。これが壊れて中の生きたマイコプラズマが放出されることもあれば、そのまま吸収されてしまうこともある。慢性例では往々にして胸郭内の癒着が認められる。 |
|||||||||
|
|||||||||
|
|||||||||
|
|
|||||||||
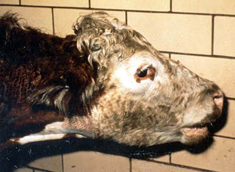
臨床診断 群中の多数の牛における急性あるいは慢性の発咳、食欲不振、体重の減少を伴う呼吸器疾患の発生 (写真 1) では、かなり牛肺疫が疑われる。重要な呼吸器症状として、速迫した、困難を伴う、騒々しい呼吸;鼻孔からの鼻汁の流出 (写真 2); 特に運動後の発咳を探す。 病理解剖所見はとても特徴的である。以下の場合には牛肺疫を強く疑うべきである: 黄色の液体が胸腔に貯溜している; 肺が黄色いもので覆われている (写真 3); 肺が胸郭に癒着している;肺がしぼまず、硬く、肝変または大理石紋様を呈している (写真 4); 慢性例ではシーケストラ (写真 5) が認められることがある。 |
|||||||||
鑑別診断 牛肺疫の臨床症状はかなり特徴的である。にもかかわらず、牛肺疫と紛らわしい多くの疾病が存在する。それらは: 牛 疫、出血性敗血症、東海岸熱、細菌性・ウイルス性気管支肺炎、急性パスツレラ感染症、牛結核、アクチノバシラス症、創傷性心膜炎、膿 瘍、包虫のシスト |
|||||||||
検査診断 組織病理学的診断も診断の一助となるが、本病の確定診断は病原体の分離と同定、及び/又は、特異的な抗原の検出あるいは適切な血清学的検査方法による抗体の検出である。 実験室における牛肺疫の診断方法の詳細は、OIE の「診断検査とワクチンの標準マニュアル」(2000 年発行第 4 版; www.oie.int に掲載)を参照されたい。以下は、通常用いるべき検査方法に重点を置いたその概要である。 検査診断のための検体の採取と輸送: MmmSC の培養と同定 抗原の検出 寒天ゲル内沈降反応--便利で簡単な検査方法--: 間接蛍光抗体法 免疫科学的検査 抗体の検出 |
|||||||||
FAO Animal Health Manual No. 14「牛肺疫 (CBPP) 緊急対応準備計画策定の手引書」をダウンロードする --> pdf file: 772 kb |
|||||||||
| Foreign Animal Diseases をダウンロードする --> pdf file: 4.4 Mb |