|
ランピー・スキン病 (lumpy skin disease: LSD)
|
||||
ランピー・スキン病 (Ngamiland disease, knopvelsiekte, maladie nodularie cutanee) は、 1929 年にザンビアで発見された牛の急性あるいは亜急性のウイルス性伝染病で、現在はアフリカ大陸のほとんどの地域に発生がある。症状は発熱、皮膚、皮下織、呼吸器および消化器粘膜における結節状硬結、四肢や下腹部皮下織における水腫、局所リンパ節の腫大で、時に結節状硬結は骨格筋にも生ずる。 |
||||
病原体 病原体は南アフリカの症例から von Backstrom によって分離された (1945 年)。本病のウイルスはポックスウイルス科 (Poxviridae)、コルドウイルス亜科 (Chordopoxvirinae) の典型的な性質を持ち、組織培養細胞では細胞質内封入体形成が見られる細胞変性効果 (cytopathic effect: CPE) を起こす。血清学的には羊痘瘡ウイルス (Capripoxvirus) とみなされている。本ウイルスは多数の哺乳類の培養細胞で増殖し、発育鶏卵でも分離が可能である。 |
||||
|
||||
感染様式および疫学 LSD は従来アフリカだけに限定発生していたが、1989 年にはイスラエルにおける発生も報告されている。ウイルスはカプリポックスに分類されるが地理的分布は緬山羊のポックスの分布と一致していない。本症は北緯 10 度以南の、雨量の多いアフリカ全域に見られる。本症の伝搬には昆虫 (節足動物) の媒介が示唆されているが、流行地では接触感染も起こっている。本症の罹患率は南アフリカでは 50 %から 100 %で、死亡率は通常 1 %であるが、時に 75 %になることもある。 LSD ウイルスの自然宿主は牛である。コブウシや外来種にも感染が成立するが、抵抗力があるため皮膚病変を形成するだけで発病することはない。アフリカ在来種は感受性が高く、全身症状と皮膚病変が見られる。成牛に比べ子牛が重篤になり、若い子牛では致死率が高い。ウイルスは血液、脾臓、唾液、精液に存在し、皮膚病変表面の浸出液の中では数日間生存している。 実験感染では、緬山羊は紅疹が現れてもすぐに消失し発病しないことから、LSD ウイルスのキャリアーとしての役割が示唆されている。狩猟動物の症例は報告されていないが、実験感染ではキリンやインパラの子は非常に感受性が高い。 LSD ウイルスは発病後、血中で 4 日間、唾液で 11 日間、精液で 22 日間および皮膚結節では少なくとも 33 日間証明される。皮膚病変の壊死乾燥物の中では 18 日間生存していた。臨床症状が消失後のウイルス血症はない。LSD ウイルスは摂氏 4 度で数ヶ月間、マイナス 80 度では数年間生存できた。 |
||||
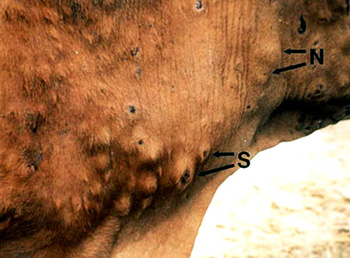
臨床症状および病理学的所見 潜伏期は実験感染例では 7 日から 14 日であるが、自然感染例は 2 週間から 5 週間以上である。発熱は特徴的な 2 相性で、特徴的皮膚病変は 2 回目の発熱時 (初回発熱後の 1 週間から 10 日目ごろ) に発現してくる。2 回目の発熱では食欲不振、流涎、流涙、鼻汁が見られる。 皮膚病変は境界明瞭で表面が扁平な硬い円形結節であり、疼痛を伴う。結節の大きさは 0.5~5 cm である。皮膚結節の数は少ない場合、数個程度である。一般には、頭部、頚部、背部、四肢、会陰部、陰嚢、乳頭、鼻鏡、および目の周囲などに無数に形成されることが多く、場合によっては全身に生ずる。結節は 7~10 日後に皮膚潰瘍を伴う壊死に陥り、後に乾燥した硬結となり、3~5 週で脱落する。皮下織の水腫は四肢、喉ぶくろ、外部生殖器などの皮膚の壊死部に生じ、数週間後、皮膚が脱落して潰瘍底が皮下織におよぶ深い皮膚潰瘍を形成する。鼻鏡や気道、口腔内や食道、および生殖器などの粘膜面にも同様な潰瘍を伴う黄灰色結節がしばしば形成される。このような深い潰瘍が四肢にできると跛行を呈することがある。 |
||||
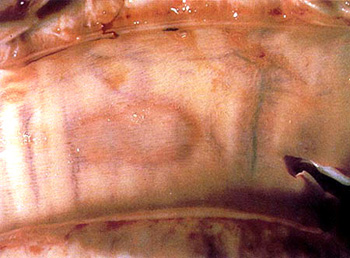
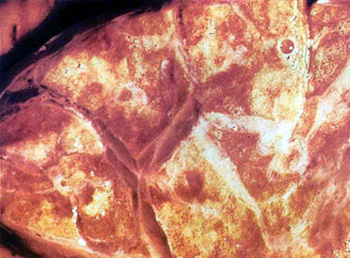
診断 急性の LSD は特徴的皮膚病変を確認して診断するが、病変が軽度の症例や非定形型では疫学情報が参考にはなるものの、臨床診断は困難である。確定診断は実験室で LSD ウイルスを証明する必要がある。すなわち組織培養細胞を用いて典型的な封入体を確認することと、中和試験によって確定診断をする。罹患動物の病理組織検査も有用であるとともに、病変部の乳剤を材料として電子顕微鏡によるウイルスの確認も重要である。 剖検では、罹患動物の皮膚結節に連続して灰白色の水腫性硬結が見られ、骨格筋、肺、第1胃、子宮などにも見られることが多い。上部気道や上部消化器の粘膜では潰瘍を伴う灰黄色壊死病変を形成する。 病理組織学的には上皮細胞、平滑筋細胞、マクロファージ、リンパ球および時に繊維芽細胞内に細胞質内封入体の形成がある。 ウイルス分離は、皮膚病変の乳剤を羊または牛の精巣細胞あるいは腎細胞などの培養細胞に接種して分離する。接種後 5 日から 15 日で特有の CPE が見られ、好酸性細胞質内封入体が見られるようになる。ウイルス粒子の確認は、病変部乳剤を蒸留水で溶解し、電子顕微鏡で観察する。大きさ 250~300 nm x 200~250 nm のワクシニアウイルス類似の形態を呈する粒子を確認する。この方法は迅速診断には非常に有効である。 ヘルペスウイルスに属するアロートンウイルスと孤児ウイルスが、しばしば LSD 様病変から分離される。従ってこれらのヘルペスウイルス感染症と LSD との類症鑑別が重要である。アロートンウイルス感染症の病変は LSD の初期病変に類似し、仮性 LSD の原因である。従ってこのヘルペスウイルスは LSD の確定診断の際に混乱を招くが、封入体の性質から識別することが可能である。すなわちヘルペスウイルスの封入体は、エオジン好性の核内封入体であるのに対し、LSD のそれはエオジン好性の細胞質内封入体で、その中央に好塩基性内体を持っている。 また、アフリカの沿岸地域の牛に見られる LSD 様病変から、しばしばウシヘルペスウイルス (BHV) 2 が分離される。このような症例はポックスウイルスによる LSD に比べて症状が軽く、仮性 LSD に類似する。このウイルス感染による症状はヘルペス乳頭炎、口内炎、および皮膚炎を主徴とすることから、LSD との重要な鑑別点である。これらヘルペスウイルスでは培養感染細胞がシンチジュームを形成すること、および好酸性核内封入体を形成することが特徴的である。 |
||||
|
||||
対策および予防 治療は現在のところ不可能である。媒介動物について詳細な研究が不足しているため、有効な予防は確立していない。間接的な方法として節足動物駆除を目的にした殺虫剤の散布、接触感染防止を目的にした罹患動物の淘汰などがある。 ワクチンは羊ポックスウイルスを子ヒツジの精巣培養細胞に感染させてワクチンとして利用する方法と、発育鶏卵で継代順化した LSD virus (Neethling virus 株) ワクチンとがある。前者のワクチンとしての評価は LSD に対して高いが、羊や山羊が同時に係留されているような場所、あるいは羊ポックスの清浄地での使用には問題が残る。 |
||||
本文は国際農林業協力協会 (AICAF) 発行「熱帯農業シリーズ 23 熱帯に多発する家畜の重要伝染病」より転載した。またここに掲載されている写真は、Foreign Animal Diseases より転載した。Foreign Animal Diseases をダウンロードする --> pdf file: 4.4 Mb |